Aufkommende Multiresistenz
Die Antibiotikabehandlung ist einer der wichtigsten Ansätze der modernen Medizin, mit dem die Ausbreitung von Infektionen verhindert werden soll. Von den 1930er bis zu den 1960er Jahren wurden viele neue Antibiotika entdeckt, was diesem Zeitraum den Namen "goldenes Zeitalter der Antibiotikaentdeckung" einbrachte. Diese Ära ist jedoch zu Ende gegangen, da das Tempo der Entdeckung neuer Antibiotika angesichts des Auftretens resistenter Krankheitserreger nicht aufrechterhalten werden konnte [1]. Die Antibiotikaresistenz stellt eine ernste und wachsende globale Bedrohung für Mensch und Tier dar. Faktoren, die mit dem Auftreten von Antibiotikaresistenzen in Verbindung gebracht werden, sind der übermäßige Einsatz von Antibiotika bei Mensch und Tier (z. B. in der Vieh- und Fischzucht), die Freisetzung von nicht metabolisierten Antibiotika in die Umwelt über Gülle und Fäkalien sowie die wachsende menschliche Bevölkerung und die globale Migration. Diese Faktoren erhöhen den Selektionsdruck auf Bakterien, was zur Entwicklung von Resistenzen durch Mutation oder den Erwerb von Resistenzgenen führt und die Verbreitung resistenter Stämme fördert. Es sind umfassende Anstrengungen erforderlich, um das Tempo der Resistenzentwicklung zu minimieren, indem uncharakterisierte Mikroorganismen und Resistenzmechanismen sowie neue antimikrobielle Wirkstoffe untersucht werden [2].
Das Helmholtz-Zentrum für Infektionsforschung
Das HZI ist Mitglied der größten deutschen Wissenschaftsorganisation, der Helmholtz-Gemeinschaft. Generell liegt der Schwerpunkt der Forschung am HZI auf der translationalen Infektionsforschung, einschließlich bakterieller und viraler Krankheitserreger, Immunabwehrmechanismen und neuartiger pharmazeutischer Wirkstoffe, einschließlich Antibiotika. Die Gruppe "Mikrobielle Wirkstoffe" unter der Leitung von Prof. Dr. Marc Stadler untersucht Sekundärmetaboliten, d.h. biologisch aktive Naturstoffe, um daraus potenzielle antimikrobielle Wirkstoffkandidaten abzuleiten. Naturstoffe sind definiert als chemische Verbindungen, die von einem lebenden System produziert werden. Nur wenige dieser komplexen Moleküle können durch Totalsynthese kosteneffizient hergestellt werden [3]. Trotz intensiver weltweiter Bemühungen ist die Produktion durch Bakterien und Pilze nach wie vor eine effiziente und erfolgreiche Strategie. Semisynthetische Ansätze, die Fermentationsprodukte modifizieren, können die Produkteigenschaften verbessern.
In der Gruppe "Mikrobielle Arzneimittel" am HZI werden Naturstoffe hauptsächlich aus Myxobakterien, Actinobakterien und filamentösen Pilzen gewonnen. Die Kultivierung solcher Organismen ist aufgrund des nicht-suspendierten Wachstums eine Herausforderung. Filamente beeinflussen die Medienviskosität und Pellets haben Konzentrationsgradienten und Massentransporteffekte. Darüber hinaus sind komplexe Medien, die oft auch Feststoffe enthalten, erforderlich, um die Produkttiter im Vergleich zu definierten Medien zu erhöhen [1, 4-5]. Viele Mikroorganismen wurden bisher noch nicht kultiviert und es gibt keine standardisierten Methoden, was die Bioprozessierung und das anschließende Scale-up zu einem schwierigen Unterfangen macht.
Automatisierung und Digitalisierung
Vor der Einführung von Lucullus® wurden Bioprozesse geplant und verwaltet sowie alle prozessrelevanten Informationen seit mehr als 20 Jahren in einer Microsoft Access-basierten Datenbank erfasst. Verbrauchsmaterialien wie Medien, Futtermittel, Supplemente und Puffer wurden nach einem etablierten, Access zugewiesenen Druckprotokoll vorbereitet und verschiedene prozessrelevante Informationen wie Organismenstämme, Kultivierungsbedingungen und die Zusammensetzung der Wachstumsmedien in der Datenbank erfasst. Im Laufe der Jahre hat sich eine große Menge an Informationen und auch Fehlern angesammelt. Mit dem Update der Computersystemsoftware auf Windows 10 war die Access-basierte Datenbank nicht mehr kompatibel. Seitdem wurden die Daten manuell verwaltet.
Im Jahr 2020 zog die Abteilung "Mikrobielle Arzneimittel" in ein neues Labor um und richtete eine neue technische Anlage ein. Mit dem anspruchsvollen Umzug war der Zeitpunkt optimal für einen technischen Sprung in die Zukunft mit der Anschaffung moderner und neuer Laborgeräte und der Ablösung der veralteten Access-basierten Datenbank. Nachdem die Anforderungen an die neue Software definiert waren, die Prozessüberwachung, Prozesssteuerung, Datenspeicherung und zusätzliche Planungs- und Auswertungsfunktionen umfassten, wurde eine umfassende Evaluation von vier möglichen Softwarelösungen durchgeführt. Mit Lucullus® fand das HZI eine ideale Lösung, die die Anforderungen voll erfüllte und darüber hinaus erweiterte SCADA-Basisfunktionalitäten bot, und mit der Securecell AG einen Partner mit profunder und langjähriger Erfahrung in der Bioprozessautomatisierung und -digitalisierung.
Lucullus® integrierte Plattformtechnologien für die Produktion von Antibiotika-Kandidaten
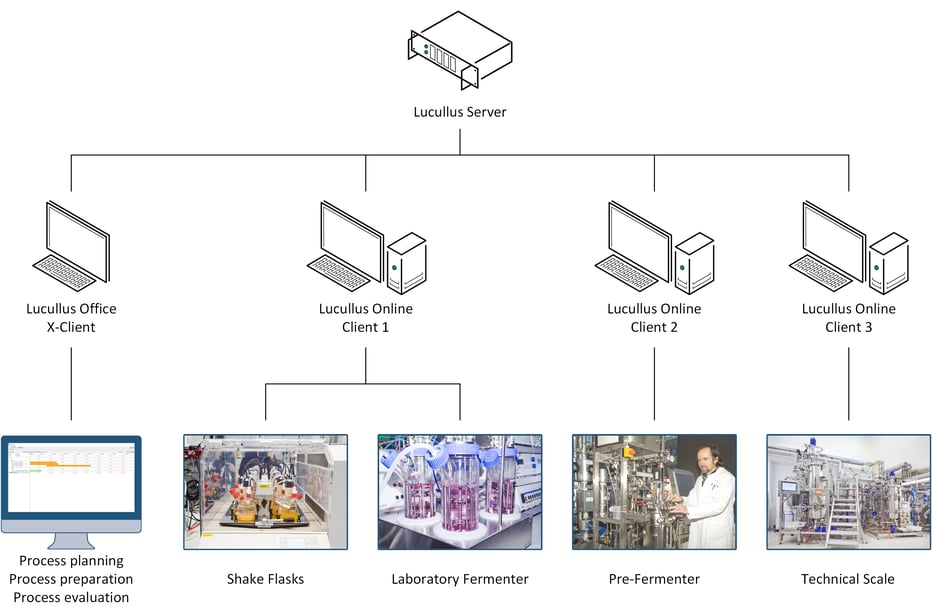
Das innovative Bioprozesslabor am HZI kombiniert Lucullus® mit mehreren integrierten modernen Mehrskalen-Fermentern, darunter RAMOS®-Schüttelkolben, Fermenter im Labormaßstab (DASGIP®-Bioreaktoren), Fermenter im kleinen Maßstab (bbi-biotech) und Bioreaktoren im technischen Maßstab (Frings), um die anspruchsvollen Kultivierungen zu bewältigen. Alle Laborgeräte einschließlich der Fermenter und Zusatzgeräte (Waagen, Pumpen) sind über das lokale Netzwerk mit der Lucullus®-Datenbank verbunden (Abbildung 1). Von einer einzigen Mensch-Maschine-Schnittstelle aus werden alle Prozessphasen einschließlich der Prozessplanung, der Prozessvorbereitung, der Prozessdurchführung und der meisten Prozessauswertungsschritte koordiniert, durchgeführt und analysiert.
Laut Miriam Grosse, Leiterin der Fermentationsanlage, besteht eine der wertvollsten Funktionen von Lucullus® darin, dass alle Prozessdaten, einschließlich der Daten von angeschlossenen Peripheriegeräten, sicher und in Echtzeit in einer zentralen Datenbank gespeichert werden, was eine vollständige Datenintegrität und lückenlose Dokumentation gewährleistet. Dies ermöglicht es den Forschern, die Daten laufender Prozesse im Lucullus®-Grafik-Tool mit den Daten historischer Prozesse zu vergleichen, um die Prozessleistung zu bewerten und Prozesse beim Upscaling zu etablieren (Abbildung 2). Mit dem Lucullus®-Planungstool werden zukünftige Bioprozesse präzise organisiert und konfiguriert, mit Reaktorauslastungsplänen, vordefinierten Prozesskontrollvorgängen, Analyseplänen und der Auswahl von Medienrezepten. Der integrierte Planungsworkflow am HZI ermöglicht eine digitalisierte und effiziente Parallelisierung von Experimenten zur Maximierung der Produktion. Anstelle eines Ausdruckprotokolls für die Medienvorbereitung werden nun im Planungstool die entsprechenden Rezepte dem Prozess zugewiesen. Im Lucullus® Media Kitchen Tool wird die Medienverwaltung und -vorbereitung durch elektronische Protokolle für die Erstellung von Medienchargen digital unterstützt. Mit dieser einzigartigen Funktion werden Bedienerfehler am HZI reduziert und eine bequeme Nachverfolgung des Rohmaterial-Footprints im Endprodukt ermöglicht.
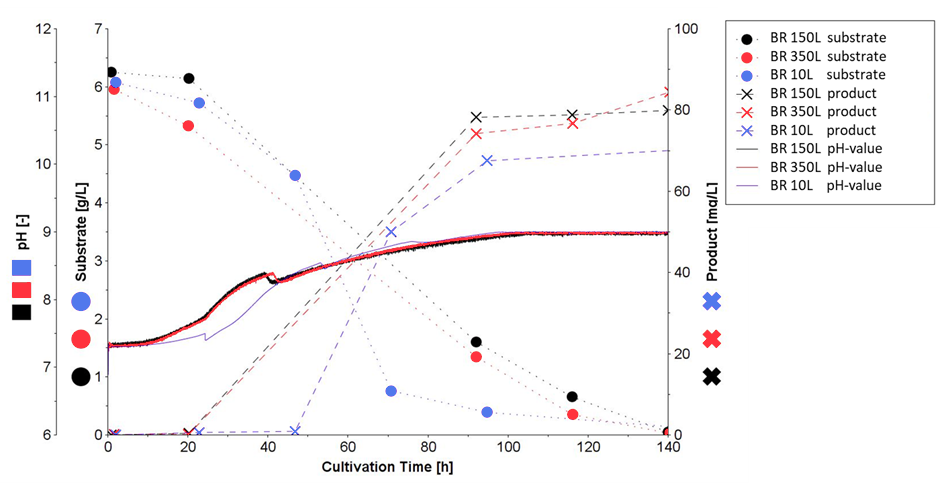 Abbildung 2: Prozess-Overlay mit einem Vergleich der historischen (10L und 150L) und der aktuell laufenden Prozesse (350L).
Abbildung 2: Prozess-Overlay mit einem Vergleich der historischen (10L und 150L) und der aktuell laufenden Prozesse (350L).
Zusammenfassung
Mit Lucullus® wurde am HZI Braunschweig eine moderne Laborumgebung digitalisiert und teilautomatisiert. Die komplexen Bioprozesse mit der Kultivierung schlecht charakterisierter Mikroorganismen zur Produktion neuartiger Naturstoffe zur Gewinnung antimikrobieller Wirkstoffkandidaten werden effizient und datenschonend überwacht und gesteuert. Die potenziellen Wirkstoffkandidaten aus Naturprodukten werden in Scale-up-Prozessen hergestellt und in präklinischen Studien mit Partnern auf ihre Wirksamkeit hin untersucht. Die am HZI am meisten geschätzte Funktion von Lucullus® ist, dass historische Daten leicht abrufbar sind und sogar mit aktuell laufenden Prozessen verglichen werden können, um schnell auf veränderte Prozessbedingungen der Pionierkultivierungen zu reagieren.
Ausblick
Für die Zukunft plant das HZI, den Einsatz von Lucullus® für die automatisierte zentrale Prozesssteuerung mit programmierbaren Abläufen zu erweitern, sobald die Prozesse besser etabliert sind. Darüber hinaus sollen optimierte Abläufe mit Attributsätzen, Sollwerten und Regelstrategien für die Routineprozesse etabliert werden. Außerdem soll eine Offline-Datenverwaltung implementiert werden. Zusammenfassend lässt sich sagen, dass Lucullus® dazu beiträgt, schwierige Kultivierungsprozesse von Mikroorganismen, die neuartige Wirkstoffe produzieren, zu etablieren und damit zu transformierenden Therapien und neuen Behandlungsmöglichkeiten beizutragen. Dieses Projekt ist in jeder Hinsicht ein Musterbeispiel. Beide Teams haben Hand in Hand gearbeitet, um eine hochmoderne Laborumgebung zu schaffen.
Referenzen
-
Miethke M, Pieroni M, Weber T, Brönstrup M, Gilbert I, Stadler M, et al. (2021) Towards the sustainable discovery and development of new antibiotics. Nat Rev Chem 5:726–749.
-
Aslam, B. et al. Antibiotic resistance: a rundown of a global crisis. Infect Drug Resist 11, 1645–1658 (2018).
-
Hanson, J. The classes of natural product and their isolation. in Natural Products: The Secondary Metabolites. Royal Society of Chemistry (ed. Hanson, J. R.) vol. 17 1–34 (The Royal Society of Chemistry, 2003).
-
Schiefer, A. et al. Corallopyronin A for short-course anti-wolbachial, macrofilaricidal treatment of filarial infections. PLoS Negl Trop Dis 14, e0008930- (2020).
-
Chaverra-Muñoz, L. & Hüttel, S. Optimization of the production process for the anticancer lead compound illudin M: process development in stirred tank bioreactors. Microb Cell Fact 21, 145 (2022).










